サリチル酸の再結晶と結晶のでき方
1 目的
サリチル酸と硫酸銅(Ⅱ)五水和物の固体混合物からサリチル酸を再結晶により分離するとともに、冷却速度の違いによるサリチル酸の結晶のでき方の違いや、加熱時と冷却時の水溶液の色の変化を観察する。
2 準備
[器具]三脚、金網、100ml三角フラスコ、50mlビーカー、50mlメスシリンダー、試験管ばさみ、漏斗、漏斗台、上皿天秤、薬包紙、薬さじ
[薬品]硫酸銅(Ⅱ)五水和物0.5g、サリチル酸1.0g
3 方法
(1) サリチル酸1.0gに不純物として硫酸銅(Ⅱ)五水和物0.5gを加え混合物とする。
(2) 三角フラスコに混合物を入れ、さらにメスシリンダーで純水を40ml加える。三角フラスコを試験管ばさみで固定し、水平に軽く振り混ぜながら加熱し、混合物を完全に溶解させる。(沸騰状態になる)
 |
 |
| 写真1 加熱前の混合物 |
写真2 加熱後溶解した混合物 |
(3) 溶解した混合物を実験台の上に移し、室温で10分間サリチル酸の結晶が析出する様子を観察する。その際、三角フラスコは静置し、初めの結晶が析出するまでの時間を正確に計る。
(4) 混合物の加熱前、加熱時、冷却後の色の変化も観察する。
(5) 三角フラスコを再び加熱して結晶を完全に溶解させる。今度は外側から水道水をかけ、急激に冷却しながらサリチル酸の結晶が析出する様子を観察する。このとき結晶析出までは三角フラスコを動かさないで水をかけ、析出後は振りながら水をかけ完全に冷やす。
(6) (5)の結晶をろ過し、10mlの水で2回洗浄する。
 |
 |
| 写真3 溶液を水道水で急冷 |
写真4 結晶ろ過 |
4 結果・考察
(1) 水溶液の色の変化 : 加熱前: 薄い青色 加熱時: 緑色 冷却後: 薄い青色
(2) 結晶析出時の観察
ア 室温でゆっくり冷却したとき
結晶析出時間:4分30秒
結晶析出の様子とその経過:初めに底に2〜3mm程度の結晶ができ、そこから針状結晶が少しずつ成長していく。
結晶1個の大きさ:約1cm〜5cm程の大きな針状結晶
 |
 |
| 写真5 結晶のでき始め |
写真6 結晶ができてから数分後 |
イ 水道水で急冷したとき
結晶析出時間:20秒
結晶析出の様子とその経過:もやもやした白い結晶が一気に析出する。
結晶1個の大きさ:約1mm以下の小さな針状結晶
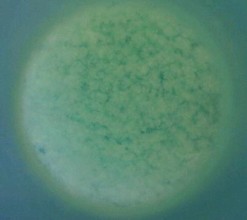 |
| 写真7 急冷後析出した結晶 |
(3) 操作(5)のろ液の色: 薄い青色 洗浄後の結晶の色: 白色
(4) 結果(2)より、より大きな結晶をつくるにはどのような条件にするとよいか。具体的にまとめよう。
| 溶液を静置してゆっくりと冷やす。例えば、魔法瓶の中に溶液を入れて結晶化する。 |
5 留意点
(1) サリチル酸と硫酸銅(Ⅱ)を用いた理由
サリチル酸は溶解度が小さく少量の試料で実験が可能であり、さらに、銅(Ⅱ)イオンとの錯形成による色変化があることによる。
(2) 硫酸銅(Ⅱ)五水和物の量は、多すぎると廃液処理の問題があり、また、少ないと溶液の青色が薄いことから0.5gとした。
(3) 操作(2)について
加える水の量は、結晶析出時間に影響を与えるので正確に量り取る。夏場では、加える水の量を少なくする方がよい。ただし、溶かす水の量を少なくすると析出時間は短縮できる反面、結晶が密集しすぎてスケッチに不向きとなる。
(4) 操作(3)について
ア 三角フラスコの中を上から常時観察する。結晶析出の最初は三角フラスコの底に2〜3mmのキズのようなものが出現する。
イ 析出時間は室温で約4〜6分である。時間を測定する意義は、よく観察させることに主眼がある。動かすと細かい結晶が析出するので、時間も変わる。
(5) 操作(4)は色の変化の観察を目的とした。なお緑色になる温度は60℃以上であり、銅(Ⅱ)イオンとサリチル酸の錯形成による。
(6) 操作(6)はサリチル酸の白い結晶のみが析出したことを確認するために行う。
6 備考
(1) 再結晶で大きな結晶をつくるには、温度が急に低下する冬場は適さない。
(2) サリチル酸と無水硫酸銅(Ⅱ)の溶解度について
7 参考文献
北海道高等学校理科研究会化学研究グループ高等学校化学実験書
北海道高等学校理科研究会(1996)









