斜方硫黄
単斜硫黄
ゴム状硫黄
形
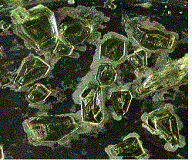


特徴
| back |
硫黄の同素体
1 目 的
硫黄は古くから知られていた元素で、火山地方には天然に単体として産するほか硫化水素や二酸化硫黄として噴出し、硫化物や硫酸塩の形でも広く存在する。そこで、硫黄の同素体をつくり、それぞれの特徴を観察し、理解を深める。
2 準 備
| 器 具 | 試験管3本、試験管立て、10mlメートルグラス、薬さじ、ペトリ皿、300mlビーカー、試験管ばさみ、三角ロート、ガラス棒、ろ紙、 マッチ、薬包紙、ルーペ |
| 試 薬 | 硫黄の粉末、二硫化炭素 |
3 方 法
| (1) | 斜方硫黄 | |
| ① | 硫黄の粉末0.2g(小さじ山盛り1杯)を試験管に取り、ドラフト内で二硫化炭素2mlを加え、ガラス棒でよくかき混ぜる。 | |
| ② | 黄色透明になるまで放置した後、ドラフト内で上澄み液をペトリ皿にあけて、ふたをわずかに開けた状態で静かに放置して、二硫化炭素を徐々に蒸発させる。 | |
| ③ | できた結晶をルーペで観察する。 | |
| (2) | 単斜硫黄 | |
| ① | 乾いた試験管に硫黄の粉末約3gを試験管に取り、振りながら上の方から均一に弱火でゆっくり加熱して融かす。このとき、温度が高すぎて硫黄が赤褐色にならないように注意する。 | |
| ② | 全部融けて黄色のさらさらした透明な液体になったところで、折り曲げてロートに入れたろ紙の中に一度に流し込む。 | |
| ③ | 表面に薄い膜ができたところで、すばやくろ紙を開いてみると、単斜硫黄の針状結晶がみられる。 | |
| ④ | できた結晶をルーペで観察する。 | |
| (3) | ゴム状硫黄 | |
| ① | 硫黄の粉末約5gを試験管に取り、振りながら強火で加熱する。加熱を続けていくと、融けてさらさらした状態(黄色透明な液体)から粘性の大きな流動性のない状態(赤褐色)に変わるが、さらに加熱を続けると再び流動性(黒褐色の液体)を示すようになる。 | |
| ② | 冷水を入れたビーカーに素早く一気に流し込む。 | |
| ③ | 生じたゴム状硫黄を水から取り出し、色・形・弾力などを観察する。 | |
4 結 果
|
斜方硫黄 |
単斜硫黄 |
ゴム状硫黄 |
|
|
形 |
 |
 |
 |
|
特徴 |
結晶がある程度の大きさに成長していれば、淡黄色斜方八面体がみられる。 | 結晶は黄色の細い針状にみえる。 | 黒色の無定型の固体で、伸ばすとゴムのように弾性を示す。 |
5 留意点
| (1) | 斜方硫黄をつくるとき使用する二硫化炭素は毒性、引火性があるので、実験はドラフト内で行い、火気には十分注意する |
| (2) | 単斜硫黄は硫黄を加熱しすぎて赤褐色にならないように十分注意する。また、ろ紙を開くタイミングが早すぎると、まだ凝固していないので液状のまま流れ出てしまうし、遅すぎると固まってしまい内部の観察ができない。 |
| (3) | ゴム状硫黄をつくるとき加熱しすぎると沸騰してしまうのでやけどをしないように注意する。硫黄は加熱中によく火がつくが、ぬれ雑巾で覆えば火は消える。このとき発生する二酸化硫黄は、有毒な気体なので吸わないように注意し、加熱はできるだけ通気性のよい場所で行う。 |
| (4) | 加熱には試験管の代わりにるつぼでもよいが、加熱の際の引火に気をつける。 |
6 備 考
加熱していけば、順次、斜方硫黄 → 単斜硫黄 → ゴム状硫黄と変化する。
| back |