混合指示薬を利用した中和滴定
1 目的
中和滴定におけるpH変化を混合指示薬の色の変化で視覚的にとらえる。また、pH参照溶液をもとに滴定曲線を作成する。
2 準備
[器具] ホールピペット(1ml,10ml)、ビュレット、ビュレット台、コニカルビーカー、漏斗、試験管、試験管立て、メートルグラス
[薬品] 0.10mol/l塩酸、0.10mol/l酢酸水溶液、0.10mol/l水酸化ナトリウム水溶液、蒸留水、混合指示薬
<混合指示薬の調整方法>
クレゾールレッド0.005g、チモールブルー0.005g、フェノールフタレイン0.10g、メチルオレンジ0.012g、ブロムチモールブルー0.060gをエタノール100mlに溶かし、 0.05mol/l水酸化ナトリウム水溶液を緑色になるまで加え、蒸留水で200mlにする。
3 方法
(1) pH参照溶液の調整
ア pH1〜pH6までの塩酸をつくる。
(ア) No.1の試験管に0.10mol/l塩酸をホールピペットで10ml入れる。
(イ) No.1の試験管から塩酸をホールピペットで1mlとり、No.2の試験管に入れる。メートルグラスで蒸留水を9mlとり、No.2の試験管に入れ全量を10mlにする。
(ウ) No.2の試験管から塩酸をホールピペットで1mlとり、No.3の試験管に入れる。メートルグラスで蒸留水を9mlとり、No.3の試験管に入れ全量を10mlにする。
(エ) この操作を繰り返して、No4、No.5、No.6の塩酸をつくる。
イ pH13〜pH8までの水酸化ナトリウム水溶液をつくる。
(ア) No.13の試験管に0.1mol/l水酸化ナトリウム水溶液をホールピペットで10ml入れる。
(イ) No.13の試験管から水酸化ナトリウム水溶液をホールピペットで1mlとり、No.12の試験管に入れる。メートルグラスで蒸留水を9mlとり、No.12の試験管に入れ全量を10mlにする。
(ウ) No.12の試験管から水酸化ナトリウム水溶液をホールピペットで1mlとり、No.11の試験管に入れる。メートルグラスで蒸留水を9mlとり、No.11の試験管に入れ全量を10mlにする。
(エ) 同様にこの操作を繰り返して、No.10、No.9、No.8の水酸化ナトリウム水溶液をつくる。
ウ No.7の試験管には蒸留水を9ml入れる。
エ No.1〜No.13の試験管に混合指示薬を2〜3滴入れて色調を比べる。
(2) 中和滴定
ア 0.10mol/l塩酸を10mlホールピペットでコニカルビーカーにとり、混合指示薬を数滴加える。
イ ビュレットに0.1mol/l水酸化ナトリウム水溶液を入れる。
ウ コックを開いてビュレットの下部に液を満たす。
エ 滴定前の目盛りを読む。
オ アの溶液にビュレットから1.0mlずつ水酸化ナトリウム水溶液を滴下し、液を軽く振り混ぜてその溶液の色を観察する。
カ 滴下量が9.5mlを過ぎた時点から注意深く水酸化ナトリウム水溶液を1滴ずつ滴下し、色が変化したときにビュレットの目盛りを読み、色を観察する。
キ 滴下量が10.5mlを過ぎた時点から11ml、12mlを滴下してその色を観察する。
ク 0.1mol/l酢酸についても同様に行う。
4 結果
(1) pH参照溶液の色調
 |
| 写真1 pH参照溶液の色調(試験管の番号はpHを表す) |
| pH(No) |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
| 色 |
赤 |
赤橙 |
橙 |
黄橙 |
黄 |
黄緑 |
緑 |
青緑 |
青 |
紫 |
赤紫 |
赤紫 |
赤紫 |
(2) 塩酸の中和滴定による指示薬の色調の変化
| 滴下量(ml) |
0 |
1.0 |
2.0 |
3.0 |
4.0 |
5.0 |
6.0 |
7.0 |
8.0 |
9.0 |
9.5 |
9.5 〜 10.5(1滴で色調が変化) |
10.5 |
11.0 |
12.0 |
| 色 |
赤 |
赤 |
赤 |
赤 |
赤 |
赤 |
赤 |
赤 |
赤橙 |
赤橙 |
橙 |
黄橙 |
黄 |
黄緑 |
緑 |
青 |
紫 |
赤紫 |
赤紫 |
赤紫 |
 |
|
 |
| 写真2 NaOHaq9.5ml滴下 |
|
写真3 NaOHaq10.0ml滴下 |
 |
|
 |
| 写真4 NaOHaq10.2ml滴下 |
|
写真5 NaOHaq10.5ml滴下 |
(3) 酢酸の中和滴定による指示薬の色調の変化
| 滴下量(ml) |
0 |
1.0 |
2.0 |
3.0 |
4.0 |
5.0 |
6.0 |
7.0 |
8.0 |
9.0 |
9.5 |
9.5 〜 10.5(1滴で色調が変化) |
10.5 |
11.0 |
12.0 |
| 色 |
橙 |
黄橙 |
黄橙 |
黄橙 |
黄橙 |
黄橙 |
黄橙 |
黄橙 |
黄橙 |
黄橙 |
黄 |
黄緑 |
緑 |
青 |
紫 |
赤紫 |
赤紫 |
赤紫 |
5 考察
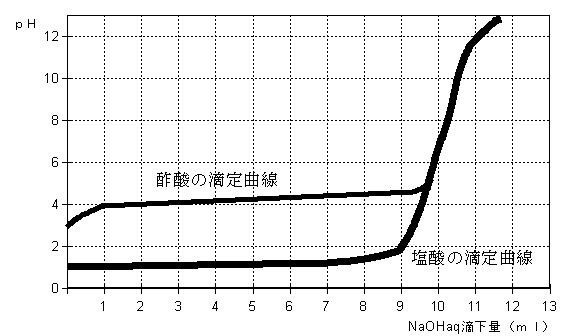
結果に基づく滴定曲線の概形
6 留意点
・中和滴定において、中和点付近では1滴で色調が変化するので、注意深く観察する。このことにより中和点付近ではpHが急激に変化することを実感できる。
・滴定曲線はpH参照溶液をもとに色調の違いにより作成するので、正確ではないが、その概形がつかめればよい。
7 参考文献
「化学実験虎の巻」日本化学会編丸善(1991)