
| back |
時計反応
1 目的
過酸化水素水でヨウ化カリウムを酸化する反応において、その反応速度に対する濃度と温度の影響を調べる。
2 原理
ヨウ化カリウムの酸化は次の式で表される。
3I- + H2O2 + 2H+ → I3- + 2H2O …(1)
反応液中に少量のチオ硫酸イオンを加えておくと、生成したI3-は、直ちに反応して、液中に現れてこない。
2S2O32- + I3- → S4O62- + 3I- …(2)
チオ硫酸イオンが消費されると次式のようにヨウ素が遊離し、デンプンと反応して溶液は青紫色になる。
I3- → I2 + I- …(3)
3 準備
| 〔器具〕 | 時計、メスシリンダー(10~20mL)、コニカルビーカーまたは大型試験管(24~30mm径)、温度計、水槽 |
| 〔薬品〕 | A液:0.10mol/L ヨウ化カリウム溶液 |
| (ヨウ化カリウム8.30gを水に溶かして500mLにする) | |
| B液:2.4×10-3mol/L チオ硫酸ナトリウム溶液 | |
| (250mLの水に1gのデンプンを加えて加熱溶解し、冷却する…a 3.0gのチオ硫酸ナトリウムを水に溶かして100mLとする…b aにb溶液10mLを加え、水を加えて500mLにする) |
|
| C液:過酸化水素水 | |
| (250mLの水に、30%過酸化水素水10mL、6mol/L酢酸16.7mLまたは氷酢酸6.0mLを加え、水を加えて500mLにする) |
4 方法
Ⅰ ヨウ化カリウムの濃度の影響
| (1) | メスシリンダーにA液(ヨウ化カリウム溶液)2.0mLを入れ、水を加えて10mLとし、コニカルビーカーに移す(写真1)。 |
 |
| (写真1) |
| (2) | コニカルビーカーにB液(チオ硫酸ナトリウム溶液)5.0mLを加えよく振り混ぜる。 |
| (3) | AとBの混合溶液にC液(過酸化水素水)5.0mLを注ぎ入れ、よく振り混ぜる。 |
| (4) | しばらくすると遊離したヨウ素がデンプンと反応して、液が青紫色に変化する(動画)。 |
| (5) | C液を加えてから、変色するまでの時間を測定する。 |
| (6) | A液の量を 4.0,6.0,8.0,10.0mLの場合も同様に行い、液が変化するのに要した時間を測定する。 |
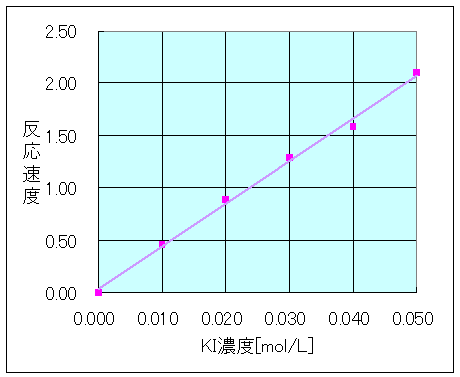
| (7) | 混合溶液中のヨウ化カリウム濃度と反応速度を計算し、その関係をグラフに表す。グラフより、比例関係が確認できる。 |
〔補足1〕 ヨウ化カリウム濃度の計算について
A,B,Cの混合溶液は20mLとなるので、
A液の体積が2.0mLのとき、濃度は10分の1となり、0.010mol/L である。
以下同様にA液の体積が4.0,6.0,8.0,10.0mLの場合、0.020,0.030,0.040,0.050mol/Lである。
〔補足2〕 反応速度の計算について
(1)式の反応速度は1秒間に生成するI3-の濃度で表すことができる。液が変化するまでの時間をtとすると、
v=[I3-]/t 〔mol/(L・s)〕
また、(2)式より、I3-は2倍のチオ硫酸イオンと反応することが分かるので、反応速度は次式で表される。
v=[Na2S2O3]/2t 〔mol/(L・s)〕
チオ硫酸ナトリウムの濃度は、B液にA液・C液を加え4倍に希釈され(B液5mL→混合溶液20mL)6.0×10-4mol/Lとなるので、上式は次のようになる。
v=6.0×10-4/2t =3.0×10-4/t 〔mol/(L・s)〕
〔実験例〕 温度19℃
| A液〔mL〕 | KI濃度〔mol/L〕 | 反応時間〔s〕 | 反応速度(v)〔×10-5mol/(L・s)〕 |
| 2.0 | 0.010 | 65.7 | 0.45 |
| 4.0 | 0.020 | 33.9 | 0.88 |
| 6.0 | 0.030 | 23.1 | 1.30 |
| 8.0 | 0.040 | 18.9 | 1.59 |
| 10.0 | 0.050 | 14.3 | 2.10 |
Ⅱ 温度の影響
(1) A液30mLに蒸留水を加えて50mLとし、0.060mol/Lヨウ化カリウム溶液を作る (A’液)。
(2) A’液10.0mLをコニカルビーカーに入れ、B液5.0mLを加える。別の試験管にC液5.0mLを取り、両者を30℃の水に5~10分間浸す(写真2)。
 |
| (写真2) |
(3) A’とBの混合溶液にC液を加え、よく振り混ぜて青紫色が現れるまでの時間を測定する。
(4) 液温が25℃,20℃、10℃について同様に測定する。
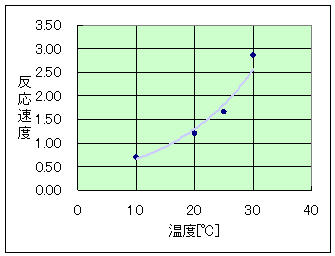
(5) 混合溶液中のヨウ化カリウム濃度と反応速度を計算し、温度と反応速度の関係をグラフに表す。
〔実験例〕
| 温度〔℃〕 | KI濃度〔mol/L〕 | 反応時間〔s〕 | v〔×10-5mol/(L・s)〕 |
| 10 | 0.030 | 42.7 | 0.70 |
| 20 | 0.030 | 25.0 | 1.20 |
| 25 | 0.030 | 18.0 | 1.67 |
| 30 | 0.030 | 10.5 | 2.89 |
5 注意事項
・B液、C液の濃度は厳密である必要はないので、ビーカーの目盛りで500mLとすればよい。
・混合溶液の量が20mLになるので、通常の試験管では溶液が混合しにくい。溶液を素早く混合するため、コニカルビーカーまたは大型試験管を用いる。なければ三角フラスコでも良い。
・この反応の速度は、酢酸酸性の下ではヨウ化カリウムと過酸化水素の濃度の積に比例するので、ヨウ化カリウム濃度を変化させる代わりに過酸化水素の濃度を変化させてもよい。
6 指導上の留意点
・この反応は、触媒(銅(Ⅱ)イオン)によって反応速度に影響を受けるので、硫酸銅(Ⅱ)溶液の量を変化させてその影響を調べるのにも利用できる。
7 参考文献
増訂 化学実験事典(赤堀史郎 木村健次郎著/講談社)
| back |