

| back |
アニリンの合成
1 目的
ニトロベンゼンのニトロ基を還元するとアニリンが生じることを理解する。
2 準備
| 器具 | 試験管、ビーカー(300ml)、三角フラスコ(100ml)、蒸発皿、駒込ピペット、三脚 、金網 |
| 薬品 | 濃塩酸、6mol/l 水酸化ナトリウム、ベンゼン、スズ粒、ジエチルエーテル、サラシ粉水溶液、ニトロベンゼン |
3 方法
| (1) 乾いた試験管にニトロベンゼン約1mlを取り、スズ粒約3gを加える。これに濃塩酸約5mlを振り混ぜながら徐々に加え、ニトロベンゼンの油滴が消え、溶液が均一になるまで温水中で加熱する。ニトロベンゼンが固まりになってしまったら、直接試験管を穏やかに加熱しながら、よく振って固まりをほぐす。 |  |
 |
| (2) スズだけを残して、反応液を100ml三角フラスコに移し、これに6mol/l 水酸化ナトリウム約30mlをかき混ぜながら徐々に加える。 |
| (3) (2)で得たアニリンの乳濁液を十分に冷やしてから、ジエチルエーテル約5mlを加え、静かに振り混ぜた後静置する。エーテルは引火しやすいので、火気に注意する。 |  |
 |
| エーテルを加える前 | エーテルを加えた後 |
| (4) 上部の黄色い液の部分をスポイトで蒸発皿に取り、熱水を入れたビーカ-の上に蒸発皿を置き、エーテルを蒸発させる。これにサラシ粉水溶液を加えて、紫色の変化を観察する。 |  |
4 備考
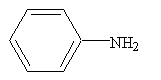
アニリン
特異臭のある無色の液体。融点-6℃、沸点184℃、空気中では徐々に赤くなり、最後には黒色不透明になる。染料や香料の原料として利用される。毒性が強く、皮膚に触れると容易に吸収され、皮膚障害、神経障害などを起こす。特に血液中に取込まれるとメトヘモグロビンを形成して、ヘモグロビンが酸素と結合しなくなる。また、沸点が高く蒸気の発生は少ないが、蒸気の許容濃度は2ppmであるので十分な注意が必要である。
| back |